T 3269:2013
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
3 用語及び定義 ··················································································································· 1
4 構成及び各部の名称 ·········································································································· 3
4.1 一般事項 ······················································································································ 3
4.2 胆すい(膵)管用ステント及びドレナージカテーテル ··························································· 3
4.3 附属品 ························································································································· 4
5 要求事項························································································································· 6
5.1 構成及び物理的要求事項 ································································································· 6
5.2 一般的要求事項 ············································································································· 8
6 包装······························································································································· 8
6.1 一次包装 ······················································································································ 8
6.2 二次包装 ······················································································································ 8
7 表示······························································································································· 8
7.1 一次包装 ······················································································································ 8
7.2 二次包装 ······················································································································ 9
7.3 図記号の使用 ················································································································ 9
附属書A(参考)力学的特性の確認試験 ·················································································· 10
附属書B(参考)腐食抵抗性の確認 ························································································ 12
T 3269:2013
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第14条によって準用する第12条第1項の規定に基づき,日本医療器材工業
会(JMED)及び一般財団法人日本規格協会(JSA)から,工業標準原案を具して日本工業規格を改正すべ
きとの申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が改正した日本工業規格である。
これによって,JIS T 3269:2007は改正され,この規格に置き換えられた。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
T 3269:2013
胆すい(膵)管用ステント及びドレナージ
カテーテル
Stents and drainage catheters for biliary and pancreatic ducts
序文
この規格は,2007年に制定されたJIS T 3269の見直しにおいて,使用者の利便性のため用語,文書構成
などの内容を変更して改正した日本工業規格である。
1
適用範囲
この規格は,長期的使用を目的として内視鏡的,経皮的,開腹術下に胆道(胆のう,胆のう管及び胆管
系)又はすい(膵)管に挿入し,排のう,排液,かん(灌)流,狭さく(窄)部位の拡張・支持,狭さく
(窄)の予防などの処置を行う胆すい(膵)管用ステント,ドレナージカテーテル及びこれら附属品の要
求事項について規定する。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,記載の西暦年の版を適用し,その後の改正版(追補を含む。)は適用しない。
JIS T 0307:2004 医療機器−医療機器のラベル,ラベリング及び供給される情報に用いる図記号
JIS T 0993-1:2012 医療機器の生物学的評価−第1部:リスクマネジメントプロセスにおける評価及
び試験
JIS T 3242:2011 非血管用ガイドワイヤ
JIS T 3243:2011 胆道用チューブ及びカテーテル
JIS T 3260:2012 カテーテル拡張器
JIS T 3261:2012 滅菌済みカテーテルイントロデューサ
JIS T 3262:2012 イントロデューサ針
3
用語及び定義
この規格で用いる主な用語及び定義は,次による。
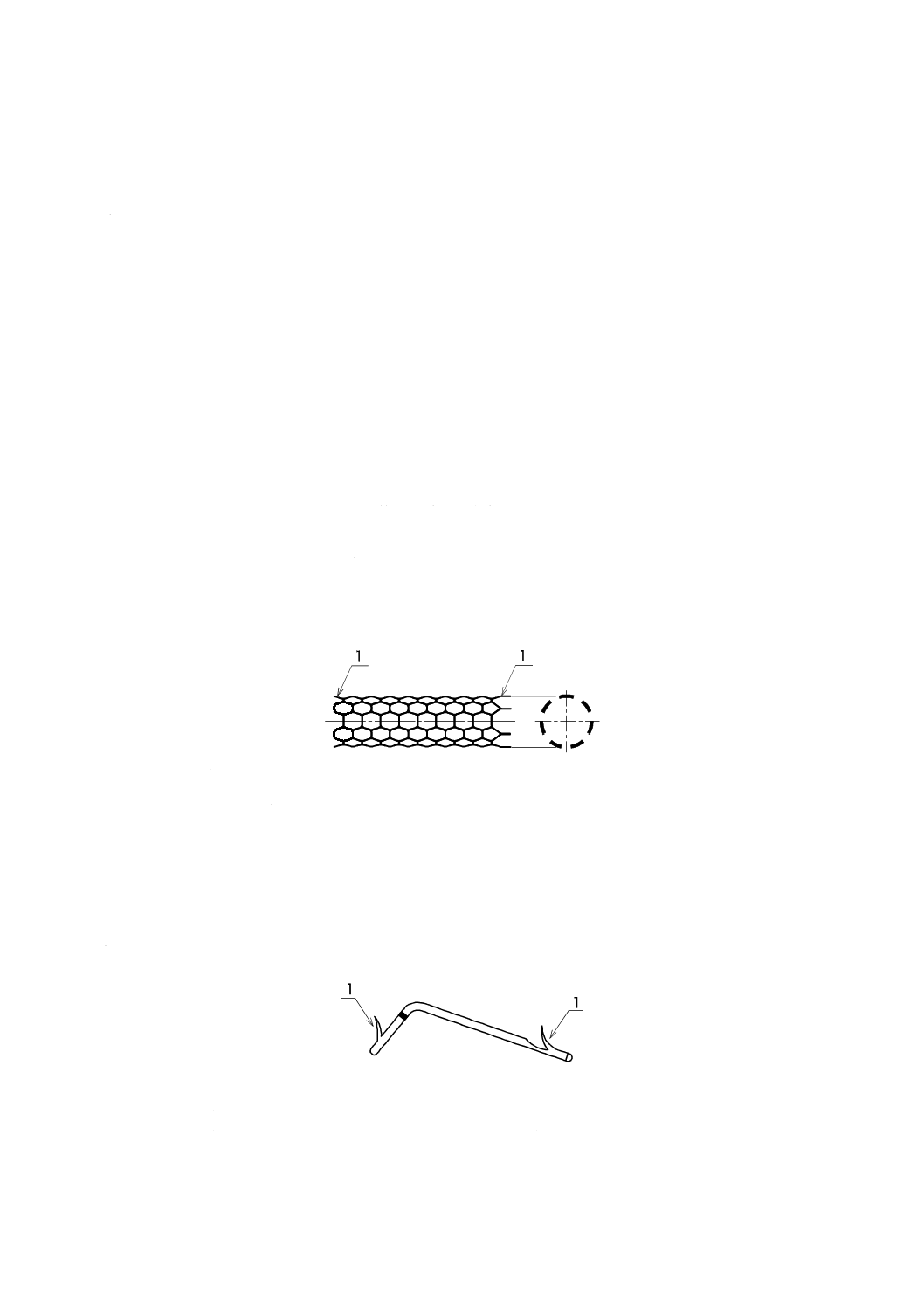
3.1
金属ステント
展開して胆管の内側にとどまる支持構造で,胆管の開存性及び通過性を維持する金属製のチューブ形の
もの(図1参照)。樹脂などで被覆したものもある。エックス線不透過性のマーカ付きのものもある。
3.2
チューブステント
2
T 3269:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
胆管又はすい(膵)管の内側にとどまる支持構造で,開存性及び通過性を維持する樹脂製のチューブ状
のもの(図2参照)。フラップ又はエックス線不透過性のマーカ付きのものもある。
3.3
ドレナージカテーテル
胆道又はすい(膵)管の排のう,排液,かん(灌)流,副子,又は狭さく(窄)防止のために使用する
柔軟なチューブ(図3及び図4参照)。内ろう用,外ろう用及び内外ろう用があり,側孔及び先端部の形
状は,様々なものがある。脱落防止機能付きのものもある(バルーン,ピッグテイル,マレコーなど)。ま
た,エックス線不透過性のマーカ付きのものもある。
3.4
デリバリーシステム
ステントと組み合わせて胆管又はすい(膵)管の狭さく(窄)部位まで挿入し,ステントの留置を行う
ために使用するイントロデューサ(図5及び図6参照)。プッシャを備えたものもある。また,先端部に
ステントをあらかじめ装着しているもの又はエックス線不透過性のマーカ付きのものもある。
3.5
バルーンカテーテル
胆管又はすい(膵)管の狭さく(窄)部位まで挿入しバルーンを拡張させることで,ステント留置を行
おうとする部位をあらかじめ拡張するための器具(図7参照)。バルーンにステントをあらかじめセット
しているもの,ステント留置のできるもの又はエックス線不透過性のマーカ付きのものもある。
3.6
最大拡張圧
バルーンの破裂,各部の漏れ,破断などが99.9 %ないことを信頼度95 %で統計的に証明できる圧力。
3.7
手元操作部
デリバリーシステムを把持し,また,デリバリーシステムの操作(ステントの留置,デリバリーシステ
ム先端部の屈伸など)を行うための部分。
3.8
ハブ
注射筒などと接続する部分。
3.9
ガイドワイヤ
デリバリーシステム,カテーテルなどの内側に通して留置部位へ誘導し,留置を容易にするための柔軟
性のある器具。操作用のトルクデバイス(ピンバイスともいう。)を備える場合がある(図8参照)。
3.10
イントロデューサ針
カテーテル,ガイドワイヤなどの配置及び操作を目的として身体に通すために用いる針(図9参照)。
3.11
ダイレータ
経皮的開口部から胆道にかけて拡張する柔軟性のある管状の器具(図10参照)。
3.12
イントロデューサ
3
T 3269:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
イントロデューサは,ダイレータとともに身体に挿入後,ダイレータを抜去してガイドワイヤ,カテー
テルなどを目的の部位に誘導できる柔軟性のあるチューブ(図11参照)。
3.13
ガイドカテーテル
ドレナージカテーテル,デリバリーシステム,バルーンカテーテル,ガイドワイヤ,ダイレータなどの
体内への挿入及び留置を補助するために用いる器具(図12参照)。
3.14
プッシャ
デリバリーシステム,ガイドワイヤなどに通し,手元側から留置部位へ押し出すことによってステント
又はカテーテルの挿入を補助する器具。
4
構成及び各部の名称
4.1
一般事項
胆すい(膵)管用ステントは,金属ステント,チューブステント及びドレナージカテーテルに区分され,
これらは,それぞれ附属品をもつ。一般的な構造及び各部の名称を,図1〜図12に示す。ただし,図1〜
図12は,一般的な構造及び名称を図示した例である。
4.2
胆すい(膵)管用ステント及びドレナージカテーテル
胆すい(膵)管用ステント及びドレナージカテーテルは,次のものがある。
a) 金属ステント(図1参照)
1 ステントの端部
注記1 デリバリーシステム又はバルーンカテーテルの先端部にあらかじめ装着
しているものもある。
注記2 構成品として,ガイドカテーテル,イントロデューサ,クリンピングチュ
ーブなどが附属する場合もある。
図1−金属ステントの例
b) チューブステント(図2参照)
1 フラップ
注記1 デリバリーシステムの先端部にあらかじめセットしているものもある。
注記2 構成品として,ストレートナ,保護チューブなどが附属する場合もある。
図2−チューブステントの例
4
T 3269:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
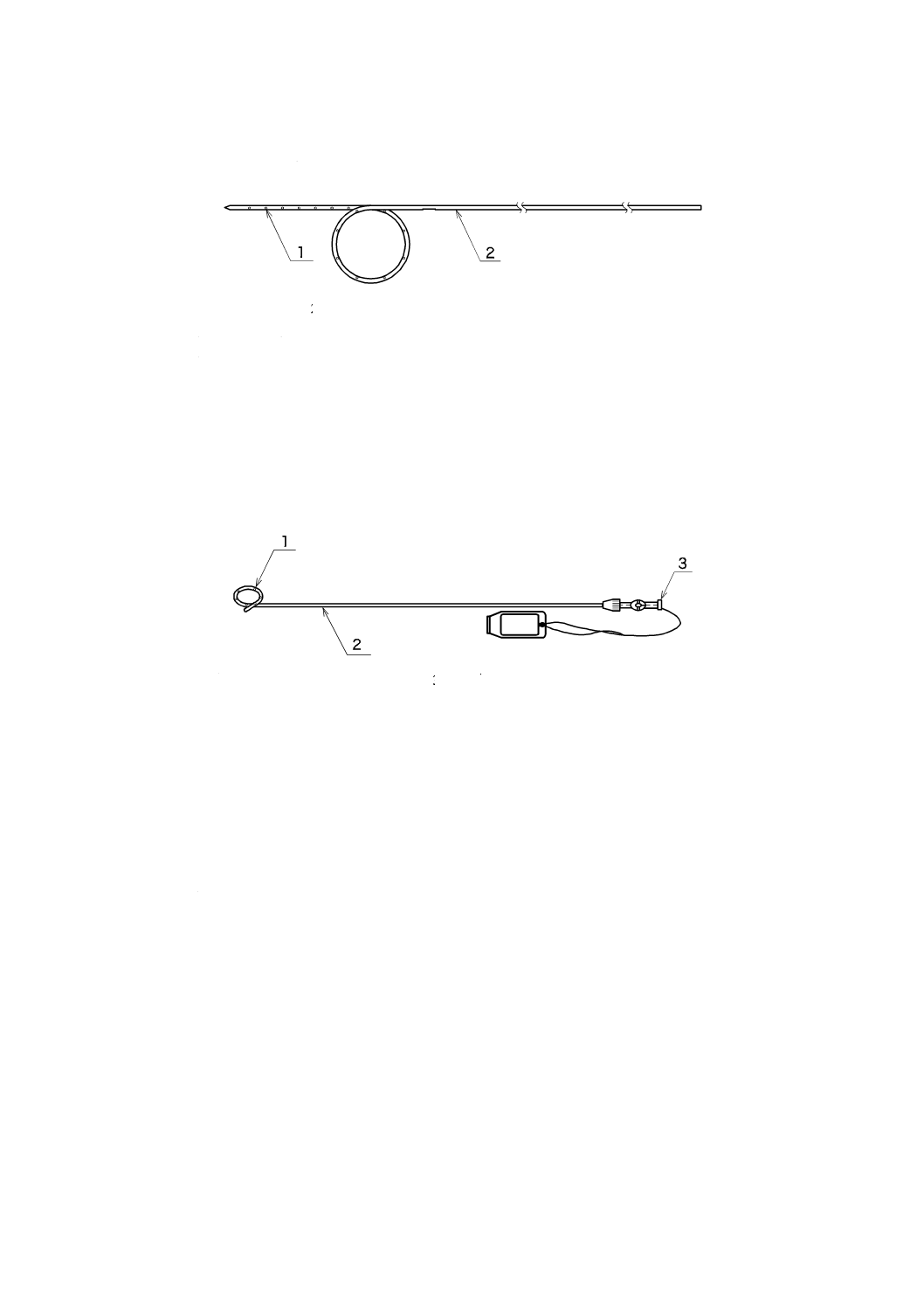
c) ドレナージカテーテル ドレナージカテーテルには,次のものがある。
1) 経内視鏡的使用タイプ(図3参照)
1 側孔 2 シャフト
注記1 脱落防止機能付きのものもある。
注記2 先端部形状,側孔の数及び位置には,様々なものがある。
注記3 構成品として,ガイドワイヤ,ダイレータ,イントロデューサ針,ガイドカテ
ーテル,プッシャ,コネクタ,活栓,イントロデューサ,トルクデバイス(ピ
ンバイス),延長チューブ,注射筒などが附属する場合もある。
図3−ドレナージカテーテル(経内視鏡的使用タイプ)の例
2) 経皮的使用タイプ(図4参照)
1 側孔 2 シャフト 3 ハブ
注記1 脱落防止機能付きのものもある。
注記2 先端部形状,側孔の数及び位置には様々なものがある。
注記3 構成品として,ガイドワイヤ,ダイレータ,イントロデューサ針,ガイドカ
テーテル,プッシャ,コネクタ,活栓,イントロデューサ,トルクデバイス
(ピンバイス),延長チューブ,注射筒などが附属する場合もある。
図4−ドレナージカテーテル(経皮的使用タイプ)の例
4.3
附属品
附属品は,次による。
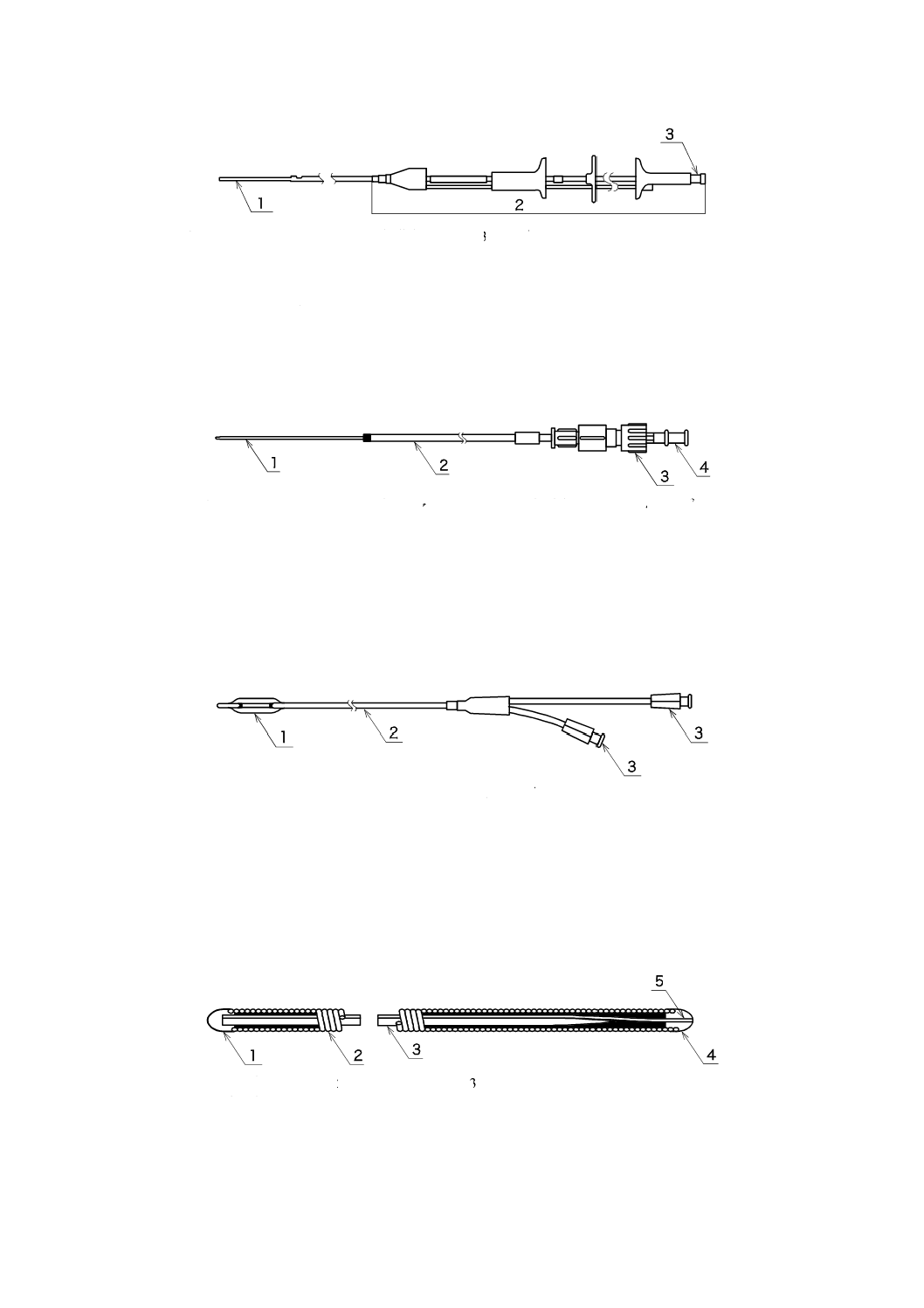
a) デリバリーシステム
1) 金属ステント用(図5参照)
5
T 3269:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
1 シャフト 2 手元操作部 3 ハブ
注記 構成品として,ガイドワイヤ,ダイレータ,イントロデューサ針,ガイドカテーテ
ル,コネクタ,活栓,イントロデューサ,トルクデバイス(ピンバイス),延長チ
ューブ,注射筒などが附属する場合もある。
図5−デリバリーシステム(金属ステント用)の例
2) チューブステント用(図6参照)
1 シャフト 2 プッシャ 3 手元操作部 4 ハブ
注記 構成品として,ガイドワイヤ,ダイレータ,イントロデューサ針,ガイドカ
テーテル,プッシャ,コネクタ,活栓,イントロデューサ,トルクデバイス
(ピンバイス),延長チューブ,注射筒などが附属する場合もある。
図6−デリバリーシステム(チューブステント用)の例
b) バルーンカテーテル(図7参照)
1 バルーン 2 シャフト 3 ハブ
注記 構成品として,ガイドワイヤ,ダイレータ,イントロデューサ針,ガイドカテー
テル,コネクタ,活栓,イントロデューサ,トルクデバイス(ピンバイス),延
長チューブ,注射筒,イントロデューサチューブなどが附属する場合もある。
図7−バルーンカテーテルの例
c) ガイドワイヤ(図8参照)
1 手元部 2 コイル 3 コアワイヤ
4 先端部 5 セーフティワイヤ
注記 構成品として,トルクデバイス(ピンバイス)などが附属する場合もある。
図8−ガイドワイヤの例
6
T 3269:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
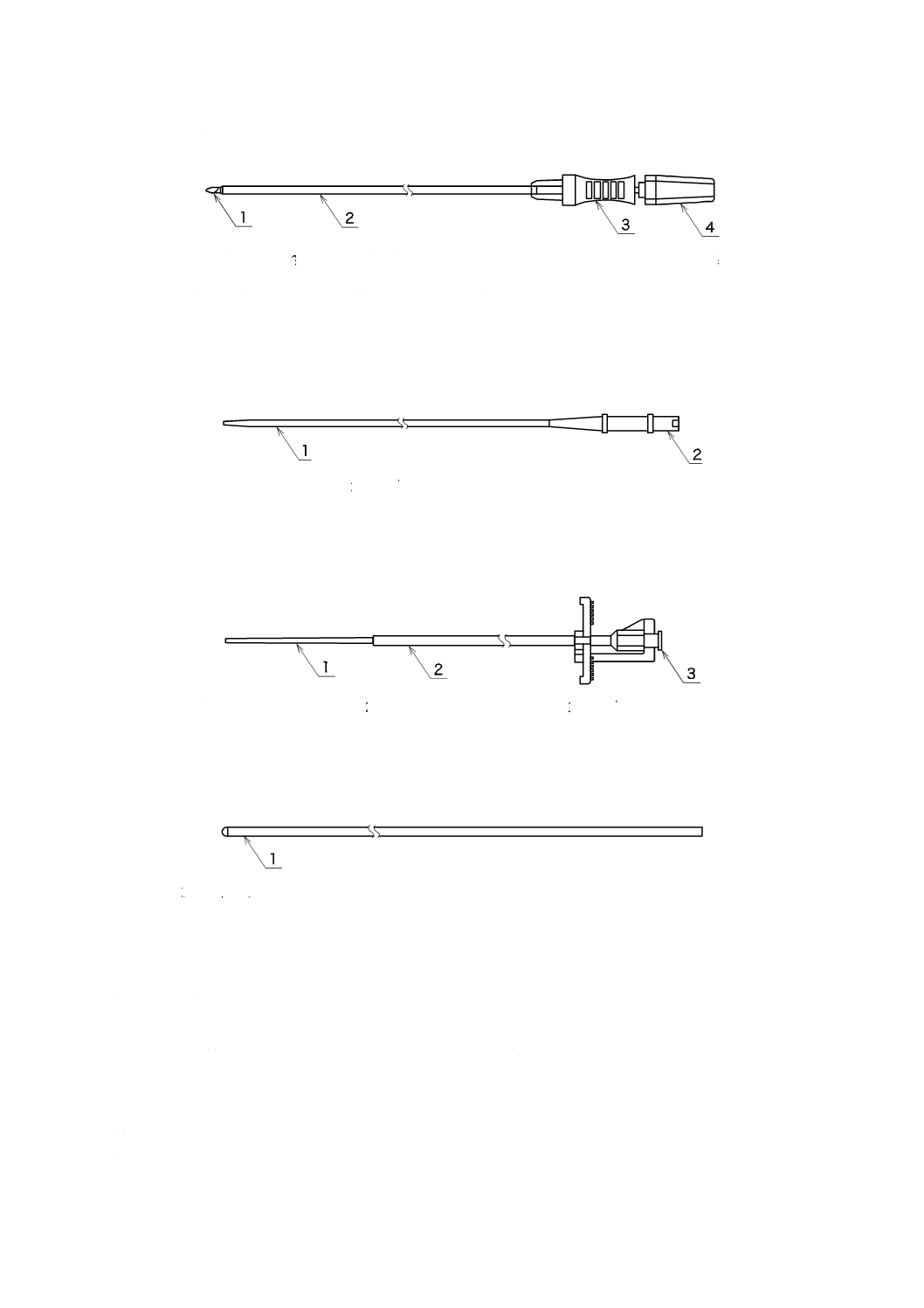
d) イントロデューサ針(図9参照)
1 針管 2 外とう(套)管(カテーテル) 3 ハブ 4 針基
注記 構成品として,保護管などが附属する場合もある。
図9−イントロデューサ針の例
e) ダイレータ(図10参照)
1 シャフト 2 ハブ
図10−ダイレータの例
f)
イントロデューサ(図11参照)
1 ダイレータ 2 イントロデューサ 3 ハブ
図11−イントロデューサの例
g) ガイドカテーテル(図12参照)
1 シャフト
図12−ガイドカテーテルの例
5
要求事項
5.1
構成及び物理的要求事項
5.1.1
構成
胆すい(膵)管用ステントである金属ステント,チューブステント又はドレナージカテーテルは,使用
目的に応じて選択された附属品とキット又はセットを構成する場合がある。金属ステント,チューブステ
ント,ドレナージカテーテル及び附属品は,該当する5.1.2〜5.1.11の要求事項に適合しなければならない。
5.1.2
金属ステント
金属ステントは,次による。
7
T 3269:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
a) 展開性 金属ステントは,添付文書の使用方法に従って操作したとき,設計された形状に展開できる
ものとする。
b) 力学的特性 金属ステントは力学的特性を確認し,使用環境で考えられる応力に対して内くう(腔)
の確保ができるものとする(附属書A参照)。
c) 腐食抵抗性 金属ステントは,金属ステントの腐食抵抗性を確認するとき,腐食の形成を認めてはな
らない(附属書B参照)。
注記 金属ステントの材料が,既に流通されているものと比べて材質が異なる場合について確認を
行う。
d) 寸法 金属ステント展開時の径及び長さは,表示値の±15 %の範囲とする。
5.1.3
チューブステント
チューブステントは,次による。
a) 引張強さ チューブステントのフラップの内側の2か所を4.9 Nの力で引っ張ったとき,破断及び亀
裂を生じてはならない。
b) 寸法 チューブステントの径及び長さは,表示値の±15 %とする。
c) 開存性 開存性は,生理食塩水,滅菌水などをチューブステントのルーメンに流し,内くう(腔)が
確保されていること,及び容易に潰れないことを確認する。
5.1.4
ドレナージカテーテル
ドレナージカテーテルは,次による。
a) 引張強さ ドレナージカテーテルの患者側と手元側とを4.9 Nの力で引っ張ったとき,破断及び亀裂
を生じてはならない。
b) 寸法 ドレナージカテーテルの径及び長さは,表示値の±10 %とする。
c) 開存性 開存性は,生理食塩水,滅菌水などをドレナージカテーテルのルーメンに流し,内くう(腔)
が確保されていることを確認する。
5.1.5
デリバリーシステム
デリバリーシステムは,シャフトと手元操作部との接合部を4.9 Nの力で引っ張ったとき,破断及び亀
裂を生じてはならない。
5.1.6
バルーンカテーテル
バルーンカテーテルは,次による。
a) 引張強さ バルーンカテーテルのシャフトとハブとの接合部を4.9 Nの力で引っ張ったとき,破断及
び亀裂を生じてはならない。
b) 耐圧性 加圧器又は注射筒をハブに接続し,バルーンを最大拡張圧まで拡張したとき,バルーンに破
裂,漏れなどの異常が99.9 %ないことを信頼度95 %にて統計学的に確認する。
なお,推奨拡張圧及び最大拡張圧は,添付文書又はラベルなどに示す。
5.1.7
ガイドワイヤ
ガイドワイヤは,JIS T 3242の箇条4(構造及び各部の名称)のa)に示す先端部の表面及びb)に示す手
元部の表面,5.1(引張強さ),7.1 a)又は7.2 d)に示す最大外径の表示に適合したものとする。
5.1.8
イントロデューサ針
イントロデューサ針は,JIS T 3262の箇条4(構成及び各部の名称)及び箇条5(要求事項)に適合した
ものとする。
8
T 3269:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
5.1.9
ダイレータ
ダイレータは,JIS T 3260の5.3(腐食抵抗性),5.4(ハブ)及び5.5(ガイドワイヤの通過性)に適合
したものとする。
5.1.10 イントロデューサ
イントロデューサは,JIS T 3261の5.3(腐食抵抗性),5.4(シースイントロデューサの要求事項)及び
5.5(ダイレータの要求事項)に適合したものとする。
5.1.11 ガイドカテーテル
ガイドカテーテルは,ガイドカテーテルの患者側と手元側とを4.9 Nの力で引っ張ったとき,破断及び
亀裂を生じてはならない。
5.2
一般的要求事項
胆すい(膵)管用ステント及びドレナージカテーテルは,附属品を含めて5.2.1〜5.2.3に適合しなければ
ならない。また,附属品を組み合わせたとき,通常の使用状態で危険の生じるおそれがないもので,かつ,
動作が円滑でなければならない。
5.2.1
外観及び清浄度
目視で検査したとき,きず,ばり又は異物の付着があってはならない。
5.2.2
生物学的安全性
JIS T 0993-1に規定する生物学的安全性の評価を行う。
5.2.3
無菌性の保証
滅菌バリデーション基準又はこれと同等以上の基準に基づき,無菌性の担保を行う。
注記 滅菌バリデーション基準には,厚生労働省が定めた滅菌バリデーション基準がある。
6
包装
6.1
一次包装
一次包装は,微生物の侵入を防止することができ,通常の取扱い,輸送及び保管中に内容製品に損傷の
おそれがないようにする。一次包装は,一度開封したら簡単に再シールできず,開封されたことが明確に
分からなければならない。
6.2
二次包装
二次包装は,通常の取扱い,輸送及び保管中に内容製品を保護できる強度をもつものとする。
7
表示
7.1
一次包装
一次包装には,次の事項を表示する。
a) チューブステント及びカテーテルの外径(mm)及び長さ(mm又はcm)。ただし,外径はミリメート
ル(mm)で示すほか,フレンチ(シャリエール),インチの呼称又はゲージを参考で併記してもよい。
注記 フレンチ(シャリエール)は,“F”,“Ch”などで表記するのがよい。円の直径1 mmが3F(Ch)
に相当し,1/3 mm刻みで表記する。ゲージは,“G”などで表記するのがよい。
b) 金属ステントの径(mm)及び長さ(mm又はcm)。ただし,ステントの径はフレンチを参考で併記し
てもよい。
c) “滅菌済み”の旨
d) 製造番号又は製造記号

9
T 3269:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
7.2
二次包装
二次包装には,次の事項を表示する。ただし,二次包装を用いず,一次包装を最小販売単位の包装とし
て用いる場合は,次の事項を一次包装に表示する。
なお,製造番号又は製造記号が滅菌年月を表示している場合は,改めて滅菌年月の表示は必要としない。
また,滅菌年月の代わりに使用期限を表示してもよい。
a) 製造業者若しくは製造販売業者の氏名又は名称,及び住所
b) 医療機器の承認番号
c) 販売名
d) チューブステント及びカテーテルの外径(mm)及び長さ(mm又はcm)。ただし,外径はミリメート
ル(mm)で示すほか,フレンチ(シャリエール),インチの呼称又はゲージを参考で併記してもよい。
注記 フレンチ(シャリエール)は,“F”,“Ch”などで表記するのがよい。円の直径1 mmが3F(Ch)
に相当し,1/3 mm刻みで表記する。ゲージは,“G”などで表記するのがよい。
e) 金属ステントの径(mm)及び長さ(mm又はcm)。ただし,ステントの径はフレンチを参考で併記し
てもよい。
f)
数量(入り数)
g) “滅菌済み”の旨
h) “再使用禁止”の旨(“ディスポーザブル”の表現は使用しない。)
i)
天然ゴムを使用しているものは,その旨。
j)
製造番号又は製造記号
k) 滅菌年月
7.3
図記号の使用
7.1及び7.2の要件は,JIS T 0307に規定する適切な図記号を使用することによってこれに替えてもよい。
注記 JIS T 0307に規定する主な図記号の例を,表1に示す。
表1−JIS T 0307に規定する主な図記号の例
10
T 3269:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書A
(参考)
力学的特性の確認試験
A.1 概要
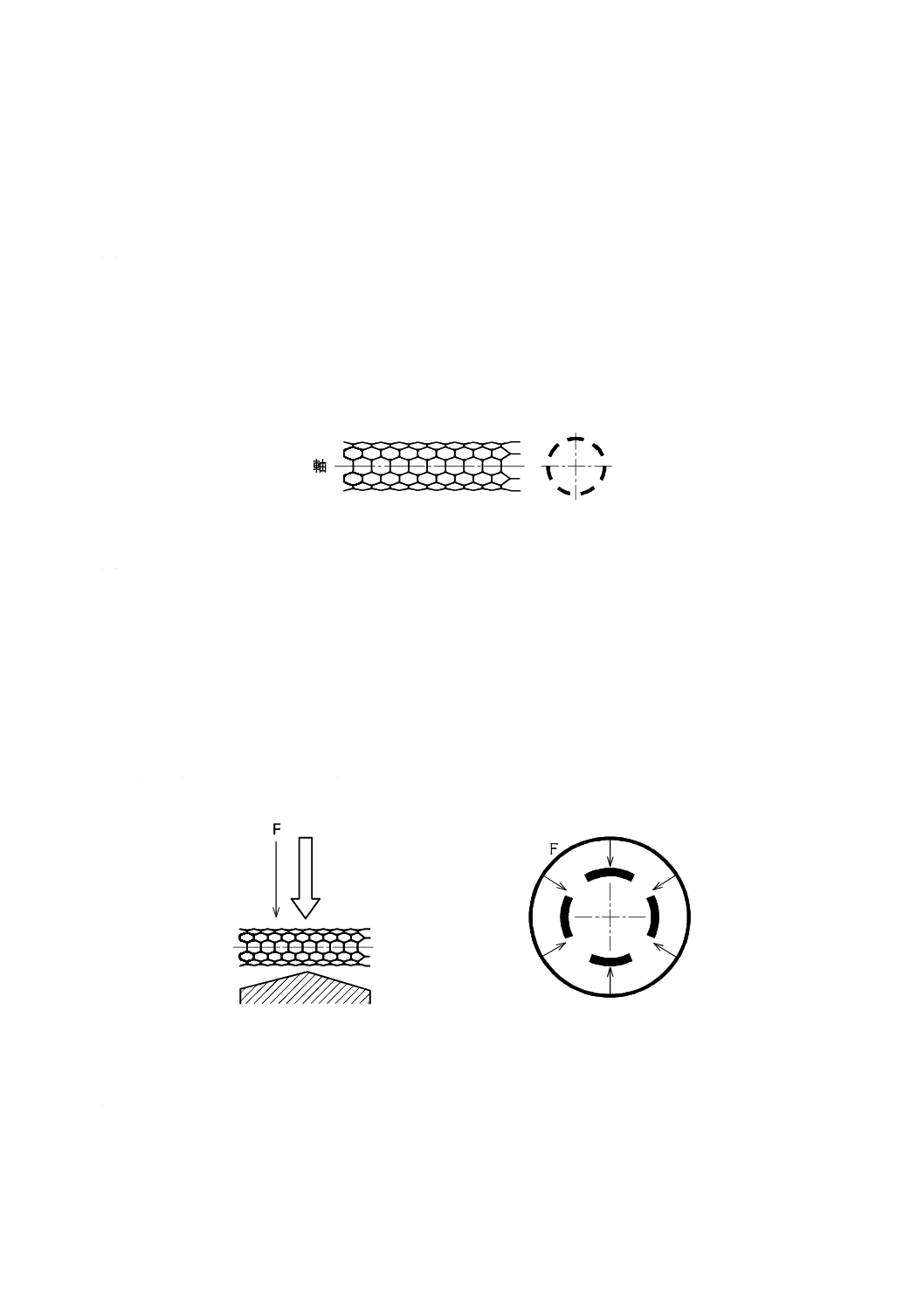
一旦展開した金属ステント(試料)に,軸と垂直方向又は軸の周囲から荷重をかけて試料を変位させ,
そのときの変位量と力を測定する。
A.2 金属ステント
金属ステントは,3.1に定義されるものをいい,図1及び図A.1に示す。
図A.1−金属ステントの軸
A.3 装置
変位量と力とを同時に測定できる装置(引張・圧縮試験機など)を用いる。
A.4 手順
試験方法は,次のいずれかを選択する(図A.2参照)。
a) 試験法1 試料の軸に対して垂直方向に荷重をかけ,試料の変位量及びそのときの力,又は試料が反
発力を失って変形したときの力を測定する。
b) 試験法2 試料の軸に対して外周から荷重をかけ,試料の変位量(収縮径)及びそのときの力,又は
試料が変形したときの力を測定する。
a) 試験法1
b) 試験法2
図A.2−金属ステントの力学試験法
A.5 試験報告書
次の項目を記載する。
a) 試料の識別
11
T 3269:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
b) 試験方法の選択
c) 試料に対する試験結果(変位量及びそのときの力,又は変形したときの力)
注記 試験報告書の記載については実測値のほか,単位当たりに換算した数値を用いてもよい。
12
T 3269:2013
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書B
(参考)
腐食抵抗性の確認
B.1
概要
金属ステントの腐食抵抗性を確認するための試験について記載する。
金属ステント(試料)を擬似胆汁液(塩基性の緩衝液など)に浸せき(漬)後,顕微鏡によって腐食の
兆候の有無を確認する。又は,電荷による負荷を試料にかけて,分極電位などから試料の耐性を確認する。
B.2
試験方法
試験は,次のいずれかの方法によって行う。
a) 浸せき(漬)試験 試験は,次による。
1) 手順 展開した検体を37±2 ℃の試験溶液[3)]に一定期間[2)]浸せき(漬)の後,蒸留水で洗
浄し,乾燥後,顕微鏡下にて判定する。
注記 加速条件下に試験を行ってもよいが,この場合には温度などの試験条件及び条件設定の根
拠を記載する。
2) 試験期間 30日以上に相当する期間
3) 試験溶液 擬似胆汁液
4) 判定 試料の表面に腐食の兆候が見られないこと。また,必要に応じて試験後の試験溶液中の構成
元素量を測定し,試料に浸食がないことを確認する。
試験報告書には,少なくとも次の事項を記載する。
− 試料の識別
− 試験方法の選択
− 試料の試験結果(試料表面の腐食の兆候の有無)
b) 電気化学試験 試験は,次による。
1) 手順 試料を脱気後37±2 ℃にした試験溶液[2)]に浸せきし,1時間の残留電位を測定する。1
時間経過後,アノード分極試験法によって電位及び電流密度を測定する。
2) 試験溶液 擬似胆汁液
3) 判定 試料及び既に流通している金属ステントで試験を行い,得られた結果を比較してチャートの
類似性,電位などから同等性に対する考察を行う。
試験報告書には,少なくとも次の事項を記載する。
− 試料の識別
− 試験方法の選択
− 外観
− 試験前後のpH
− 分極電位のチャート図





