T 3211-10:2019
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
序文 ··································································································································· 1
1 適用範囲························································································································· 1
2 引用規格························································································································· 1
2A 用語及び定義 ················································································································ 2
3 材料······························································································································· 2
4 物理的要求事項 ················································································································ 2
4.1 気泡の回避 ··················································································································· 2
4.2 微粒子汚染 ··················································································································· 2
4.3 引張強さ ······················································································································ 2
4.4 気密性 ························································································································· 3
4.5 めす(雌)及び/又はおす(雄)かん(嵌)合部の付いた接続部品 ········································· 3
4.6 保護キャップ ················································································································ 3
4.7 活栓の操作性 ················································································································ 3
4.8 混注部 ························································································································· 3
4.9 逆止弁 ························································································································· 3
5 化学的要求事項 ················································································································ 3
6 生物学的安全性 ················································································································ 3
6.1 無菌性 ························································································································· 3
6.2 発熱性 ························································································································· 3
6.3 溶血性 ························································································································· 3
7 包装······························································································································· 3
8 表示······························································································································· 3
8.1 一般 ···························································································································· 3
8.2 一次包装 ······················································································································ 4
8.3 二次包装 ······················································································································ 4
附属書A(規定)物理的試験 ·································································································· 5
附属書B(規定)化学的試験 ·································································································· 6
附属書C(規定)生物学的試験 ······························································································· 7
附属書JA(参考)JISと対応国際規格との対比表 ······································································· 8
T 3211-10:2019
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法第12条第1項の規定に基づき,一般社団法人日本医療機器テクノロジー協会
(MTJAPAN)及び一般財団法人日本規格協会(JSA)から,工業標準原案を具して日本工業規格を制定す
べきとの申出があり,日本工業標準調査会の審議を経て,厚生労働大臣が制定した日本工業規格である。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣及び日本工業標準調査会は,このような特許権,出願公開後の特許出願及び実
用新案権に関わる確認について,責任はもたない。
JIS T 3211の規格群には,次に示す部編成がある。
JIS T 3211-4 第4部:自然落下式単回使用滅菌済み輸液セット
JIS T 3211-5 第5部:単回使用滅菌済み定量筒輸液セット
JIS T 3211-8 第8部:ポンプ用単回使用滅菌済み輸液セット
JIS T 3211-9 第9部:単回使用滅菌済みチューブ
JIS T 3211-10 第10部:単回使用滅菌済み輸液チューブの附属品
JIS T 3211-11 第11部:単回使用滅菌済み輸液フィルタ
JIS T 3211-12 第12部:単回使用滅菌済み逆止弁
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格 JIS
T 3211-10:2019
滅菌済み輸液セット−
第10部:単回使用滅菌済み輸液チューブの附属品
Sterile infusion administration set-
Part 10: Sterile accessories for fluid lines for single use
序文
この規格は,2015年に第2版として発行されたISO 8536-10を基とし,我が国の実情に合わせるため,
技術的内容を変更して作成した日本工業規格である。
なお,この規格で点線の下線を施してある箇所は,対応国際規格を変更している事項である。変更の一
覧表にその説明を付けて,附属書JAに示す。
1
適用範囲
この規格は,JIS T 3211-4に規定する自然落下式輸液セットに使用する単回使用減菌済み輸液チューブ
の附属品及びJIS T 3211-8に規定するポンプ用輸液セットに使用する単回使用滅菌済み輸液チューブの附
属品(以下,附属品という。)について規定する。
この規格は,次の機器を包含する。
a) 二方活栓(two-way stopcocks,2SC),三方活栓(three-way stopcocks,3SC),四方活栓(four-way stopcocks)
及び多連活栓(stopcocks manifold,SM)
注記1 活栓の表記は,接続部の数によっている。機能部位となる場所の数は,斜線の次に活栓と
なり得る部位の数を用いて補助的記号を加えることで表すことができる。3/4−活栓は,4
か所の機能部位をもつ三方活栓を指している。
b) 混注部(UIS)
c) ストッパ又は接続部品(アダプタ)
注記2 この規格の対応国際規格及びその対応の程度を表す記号を,次に示す。
ISO 8536-10:2015,Infusion equipment for medical use−Part 10: Accessories for fluid lines for
single use with pressure infusion equipment(MOD)
なお,対応の程度を表す記号“MOD”は,ISO/IEC Guide 21-1に基づき,“修正している”
ことを示す。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格のうちで,西暦年を付記してあるものは,記載の年の版を適用し,その後の改正版(追補を含む。)
は適用しない。西暦年の付記がない引用規格は,その最新版(追補を含む。)を適用する。
JIS T 3211-4 滅菌済み輸液セット−第4部:自然落下式単回使用滅菌済み輸液セット
2
T 3211-10:2019
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注記 対応国際規格:ISO 8536-4,Infusion equipment for medical use−Part 4: Infusion sets for single use,
gravity feed(MOD)
JIS T 3211-8 滅菌済み輸液セット−第8部:ポンプ用単回使用滅菌済み輸液セット
注記 対応国際規格:ISO 8536-8,Infusion equipment for medical use−Part 8: Infusion sets for single use
with pressure infusion apparatus(MOD)
JIS T 3211-12 滅菌済み輸液セット−第12部:単回使用滅菌済み逆止弁
注記 対応国際規格:ISO 8536-12,Infusion equipment for medical use−Part 12: Check valves(MOD)
ISO 15223-1,Medical devices−Symbols to be used with medical device labels, labelling and information to be
supplied−Part 1: General requirements
ISO 80369-7:2016,Small-bore connectors for liquids and gases in healthcare applications−Part 7: Connectors
for intravascular or hypodermic applications
2A 用語及び定義
この規格で用いる主な用語及び定義は,JIS T 3211-4によるほか,次による。
2A.1
活栓
液体の流路を切換える機器。
2A.2
ストッパ
輸液の導管等の流路を開放又は閉塞状態にする機能をもつ部材。
2A.3
接続部品
医療機器同士又は部品同士をつなぐために用いる部材。アダプタともいう。
3
材料
附属品の材料は,箇条4〜箇条6の規定に適合しなければならない。
4
物理的要求事項
4.1
気泡の回避
附属品の全ての構成品は,A.1に規定する試験を行ったときに,流路に気泡を発生しないように設計し
なければならない。
4.2
微粒子汚染
附属品は,微粒子汚染を最小限に抑えた環境下で製造しなければならない。内部表面は,平滑で清浄で
なければならない。A.2に規定する試験を行ったときに,微粒子の数は,汚染指標を超えてはならない。
4.3
引張強さ
A.3に規定する試験を行ったときに,構成品間の附属品及び接続部は,15 N以上の引張力に15秒間耐え
なければならない。
活栓の場合は,プラグとハウジング間との接合は,どの位置においても,この力に耐えなければならな
い。
3
T 3211-10:2019
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
4.4
気密性
附属品は,空気,微生物及び液体が不浸透でなければならない。また,空気又は水の漏れがないもので
なければならない。活栓は,どのプラグ位置でも固定できなければならない。A.4に規定する試験を行っ
たときに,空気又は水が漏れてはならない。
4.5
めす(雌)及び/又はおす(雄)かん(嵌)合部の付いた接続部品
接続部品は,ISO 80369-7に適合しためす(雌)かん(嵌)合部の付いた接続部及び/又はおす(雄)
かん(嵌)合部の付いた接続部を提供しなければならない。
4.6
保護キャップ
JIS T 3211-4に適合しなければならない。
4.7
活栓の操作性
活栓及び多連活栓は,A.5に規定する試験を行ったときに,接近する構成品の機能に有害な影響を及ぼ
さずに流路の開閉ができるようにしなければならない。
4.8
混注部
混注部は,混注を可能にするものでなければならない。A.6に規定する試験を行ったときに,混注部は,
バッチ全ての混注部を合わせて10滴を超えて漏れてはならず,かつ,1混注部当たり2滴を超えて漏れて
はならない。
4.9
逆止弁
JIS T 3211-12に規定する試験を行ったときに,逆止弁は,水の漏れをしっかりと防ぐように閉まらなけ
ればならない。
5
化学的要求事項
JIS T 3211-4に適合しなければならない。試験方法は,附属書Bによる。
6
生物学的安全性
生物学的安全性は,附属書Cによる。
6.1
無菌性
JIS T 3211-4に適合しなければならない。
6.2
発熱性
附属品は,適切な試験を用いて発熱性物質がないことを評価しなければならない。その結果として,附
属品は,発熱性物質がないことを示さなければならない。JIS T 3211-4に適合しなければならない。
6.3
溶血性
JIS T 3211-4に適合しなければならない。
7
包装
JIS T 3211-4に適合しなければならない。
8
表示
8.1
一般
表示には,8.2及び8.3に規定している要求事項を含まなければならない。図記号を使用する場合は,ISO
15223-1による。
4
T 3211-10:2019
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注記 影響ある物質の存在は,その物質の略語“XXX”を変更し,ISO 7000の図記号2725を使用し
て示すことができる。影響ある物質がないことを,個々の記号に斜線を入れることで示すこと
ができる。
8.2
一次包装
一次包装には,少なくとも次の情報を表示しなければならない。
a) 製造販売業者の氏名又は名称及び住所
b) 包装内の内容物の説明。例えば,単回使用多連活栓。
c) 適切な文言,又はISO 15223-1に規定する図記号を用いた“滅菌済み”の表示
d) “LOT”の文字を前置きしたロット(バッチ)の表記,又はISO 15223-1に規定する図記号を用いた
ロット(バッチ)の表記
e) 適切な用語,又はISO 15223-1に規定する図記号を用いた使用期限の年月
f)
単回使用の附属品であることの表示。同等の文言,又はISO 15223-1に規定する図記号を用いての表
示でもよい。
g) 使用上の注意。添付文書でもよい。
上記情報の判読可能な文字及び/又は記号を記載するために使用できる場所が小さい場合は,d) 及び
e) だけでもよい。この場合,この細分箇条で要求する情報は,二次包装に表示しなければならない。
8.3
二次包装
二次包装には,少なくとも次の情報を表示しなければならない。
a) 製造販売業者の氏名又は名称及び住所
b) 包装内の内容物の説明。例えば,単回使用多連活栓。
c) 適切な文言,又はISO 15223-1に規定する図記号を用いた“滅菌済み”の表示
d) “LOT”の文字を前置きしたロット(バッチ)の表記,又はISO 15223-1に規定する図記号を用いた
ロット(バッチ)の表記
e) 適切な用語,又はISO 15223-1に規定する図記号を用いた使用期限の年月
f)
“ポンプ用輸液セットに安全に使用できる。”の表示
g) 入り数
h) 保管条件
5
T 3211-10:2019
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書A
(規定)
物理的試験
A.1 気泡
通常の使用条件と同じようにして,附属品に蒸留水を満たす。気泡の存在を,透明な構成品の流路につ
いて,目視で検査する。
A.2 微粒子汚染試験
洗浄液は,試験検体の内容積の50倍以上でなければならない。試験は,JIS T 3211-4に規定している方
法で行わなければならない。
A.3 引張強さ試験
附属品の長手方向に,引張力15 Nを15秒間かける。活栓は,そのプラグの回転軸方向に同じ力を,更
に加えなければならない。接合部及び部品が,試験の力に耐えるかを観察する。
A.4 気密性試験
A.4.1 試験開始時には,全ての試験システムの温度を試験温度と同じにしなければならない。
A.4.2 開口部を閉じ,ISO 80369-7に適合したおす(雄)又はめす(雌)かん(嵌)合部を用いて附属品
を空気供給装置に接続する。附属品に対し,50 kPaの内部過圧を15秒間加える。40 ℃±1 ℃の水中で,附
属品の全ての空気漏れを観察する。
A.4.3 蒸留水で附属品を満たす。附属品に対し200 kPaの圧力を15分間加える。40 ℃±1 ℃で附属品の
全ての水漏れを観察する。
A.5 活栓の操作性試験
全てのプラグを,全ての機能位置ヘ動かす。プラグの動作によって,隣接する構成品が逆に作用するか,
又は間違った調整をするかを観察する。
A.6 混注部単位の試験
JIS T 3211-4のA.5に適合しなければならない。ただし,内部圧力は200 kPaとする。
6
T 3211-10:2019
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書B
(規定)
化学的試験
B.1
試験液の調製
表面積100 cm2相当の部品を用いる。滅菌し,使用の準備ができた附属品の液体と接する部品を分解す
る。その後,同一の材質に従いそれらの部品を整理する。
全ての内部及び外部表面が浸せきする大きさに部品を裁断する。250 mLの口広の三角フラスコへ入れ,
最新版の日本薬局方で規定する蒸留水を200 mL加える。フラスコに蓋をして,37 ℃±1 ℃で24時間放置
する。
他の三角フラスコへ最新版の日本薬局方で規定する蒸留水200 mLを入れ,フラスコに蓋をして,37 ℃
±1 ℃で24時間放置する。この液は,JIS T 3211-4に従った試験の対照溶液として使用する。
B.2
試験手順
試験は,JIS T 3211-4の箇条7の規定に従って行わなければならない。ただし,試験液は,B.1に規定す
る試験液を使用する。
7
T 3211-10:2019
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書C
(規定)
生物学的試験
C.1 生物学的試験
JIS T 3211-4の附属書Cに適合しなければならない。
参考文献
[1] ISO 11135-1:2007,Sterilization of health care products−Ethylene oxide−Part 1: Requirements for
development, validation and routine control of a sterilization process for medical devices
[2] JIS T 0806-1 ヘルスケア製品の滅菌−放射線−第1部:医療機器の滅菌プロセスの開発,バリデーシ
ョン及び日常管理の要求事項
注記 原国際規格では,ISO 11137-1,Sterilization of health care products−Radiation−Part 1:
Requirements for development, validation and routine control of a sterilization process for medical
devicesを記載している。
[3] ISO 11137-2,Sterilization of health care products−Radiation−Part 2: Establishing the sterilization dose
[4] JIS T 0816-1 ヘルスケア製品の滅菌−湿熱−第1部:医療機器の滅菌プロセスの開発,バリデーショ
ン及び日常管理の要求事項
注記 原国際規格では,ISO 17665-1,Sterilization of health care products−Moist heat−Part 1:
Requirements for the development, validation and routine control of a sterilization process for
medical devicesを記載している。
[5] EN 15986,Symbol for use in the labelling of medical devices−Requirements for labelling of medical devices
containing phthalate
[6] European Pharmacopoeia
[7] United States Pharmacopeia
[8] 日本薬局方
[9] ISO 7000,Graphical symbols for use on equipment−Registered symbols
8
T 3211-10:2019
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
附属書JA
(参考)
JISと対応国際規格との対比表
JIS T 3211-10:2019 滅菌済み輸液セット−第10部:単回使用滅菌済み輸液チュ
ーブの附属品
ISO 8536-10:2015,Infusion equipment for medical use−Part 10: Accessories for fluid
lines for single use with pressure infusion equipment
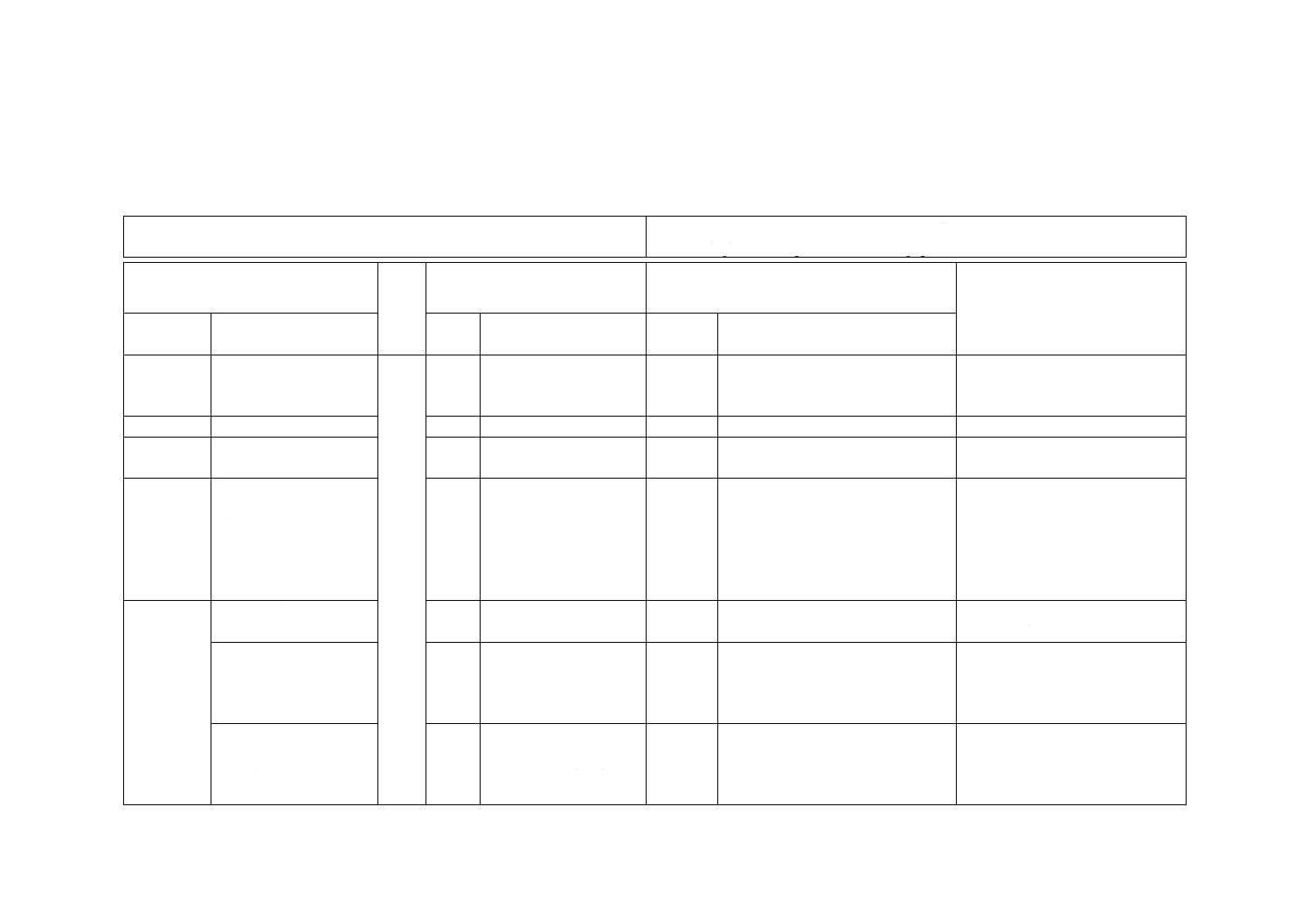
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごと
の評価及びその内容
(V)JISと国際規格との技術的差
異の理由及び今後の対策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
1 適用範囲
−
1
一部の国では,ISO
8536-10よりも法規が優
先される。
削除
この規格では,削除した。
各国の対応についての記載のた
め,削除した。
2 引用規格
2A 用語及
び定義
3項目の用語及び定義を
記載
−
−
追加
ISO規格には用語及び定義の箇条
はない。
利用者の利便性のため,実質的な
差異はない。
4 物理的要
求事項
4.5 めす(雌)及び/又
はおす(雄)かん(嵌)
合部の付いた接続部品
ISO 80369-7に適合した
めす(雌)かん(嵌)合
部
4.5
ISO 594-2に適合しため
す(雌)かん(嵌)合部
変更
この規格では,ISO 80369-7へ変更
した。
最新のISO 80369-7だけを適用す
るように変更した。
6 生物学的
安全性
生物学的安全性は,附属
書Cによる。
−
−
追加
この規格では,附属書Cを追加し
た。
この規格では,附属書Cを引用す
る記載を追記した。
6.1 無菌性
JIS T 3211-4に適合しな
ければならない。
6
6.1 無菌性
バリデーションされた
滅菌プロセスを受けな
ければならない。
変更
この規格では,JIS T 3211-4への適
合とした。
JIS T 3211規格群として整合を図
る。技術的差異はない。
6.3 溶血性
JIS T 3211-4に適合しな
ければならない。
6.3 溶血性
溶血性試験をしなけれ
ばならない。試験方法は
ISO 10993-4による。
変更
この規格では,JIS T 3211-4への適
合とした。
JIS T 3211規格群として整合を図
る。技術的差異はない。
2
T
3
2
11
-1
0
:
2
0
1
9
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
9
T 3211-10:2019
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
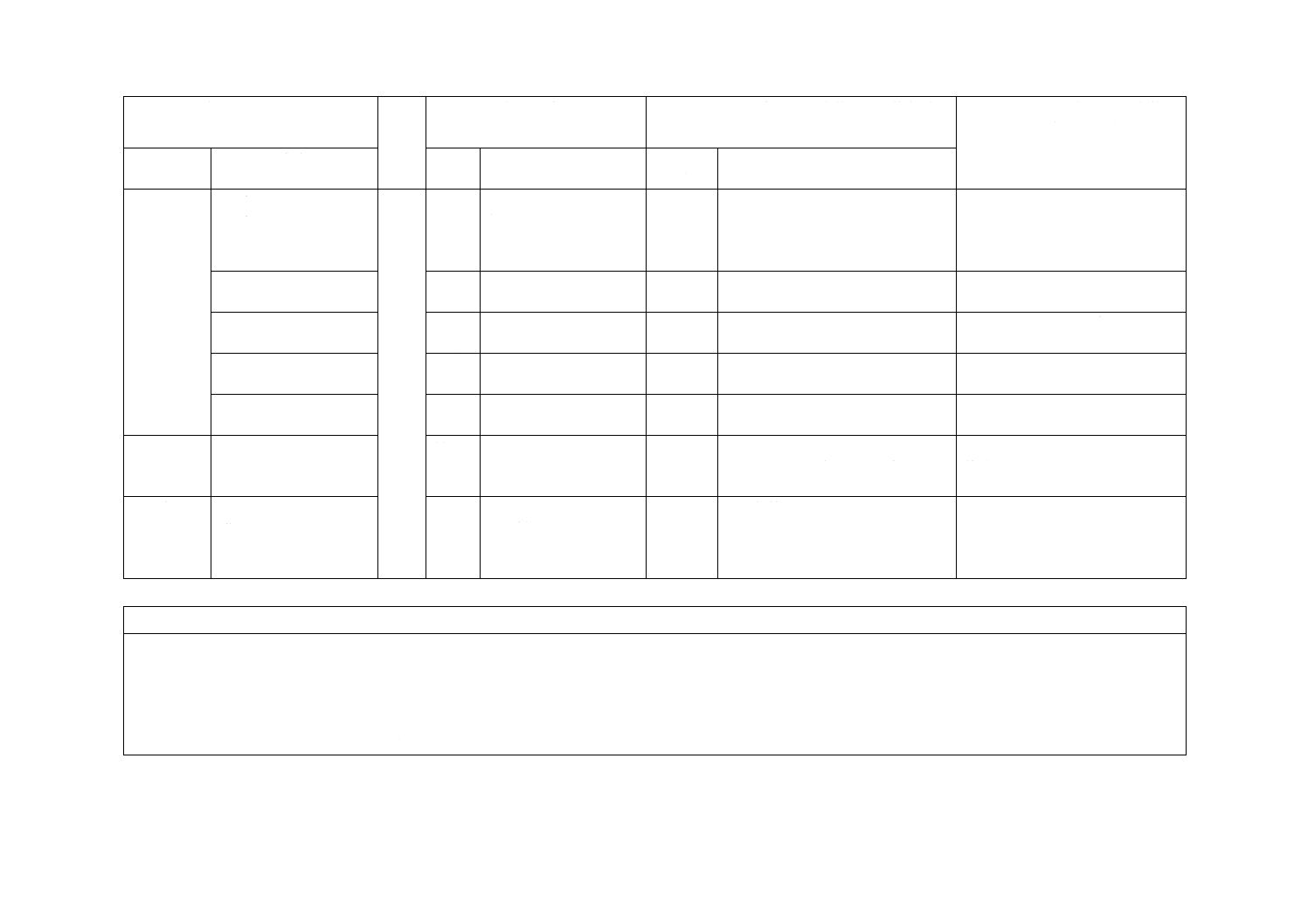
(I)JISの規定
(II)
国際
規格
番号
(III)国際規格の規定
(IV)JISと国際規格との技術的差異の箇条ごと
の評価及びその内容
(V)JISと国際規格との技術的差
異の理由及び今後の対策
箇条番号
及び題名
内容
箇条
番号
内容
箇条ごと
の評価
技術的差異の内容
8 表示
8.2 a)
8.3 a)
製造販売業者の氏名又
は名称及び住所
8.2
8.3
a) 製造業者の名前及び
住所
変更
この規格では,医薬品医療機器等法
に従った記載とした。
技術的差異はない。
−
8.2 c)
発熱性及びエンドトキ
シンがないことの表示
削除
この規格では,削除した。
医薬品医療機器等法上も要求がな
いことから削除した。
−
8.2 j)
8.3 f)
Pの表示
削除
この規格では,削除した。
PaediatricのPとの間違いの可能性
を考慮し,削除した。
8.3 c)
滅菌済みの表示
−
−
追加
この規格では,滅菌済みの表示を追
加した。
JIS T 3211規格群の他の規格と整
合を図るため追加した。
8.3 g)
入り数
−
−
追加
この規格では,二次包装の表示とし
て“入り数”を追加した。
JIS T 3211-4と整合を図るため追
加した。
−
−
11
廃棄に関する規定
削除
廃棄物処理法で規定されているこ
とから,この規格では,不採用とし
た。
我が国では,不採用とした。技術
的差異はない。
附属書A
(規定)
A.4.2
ISO 80369-7に適合した
おす(雄)又はめす(雌)
かん(嵌)合部
A.4.2
ISO 594-2に適合したお
す(雄)又はめす(雌)
かん(嵌)合部
変更
この規格では,ISO 80369-7へ変更
した。
最新のISO 80369-7だけを適用す
るように変更した。
JISと国際規格との対応の程度の全体評価:ISO 8536-10:2015,MOD
注記1 箇条ごとの評価欄の用語の意味は,次による。
− 削除 ················ 国際規格の規定項目又は規定内容を削除している。
− 追加 ················ 国際規格にない規定項目又は規定内容を追加している。
− 変更 ················ 国際規格の規定内容を変更している。
注記2 JISと国際規格との対応の程度の全体評価欄の記号の意味は,次による。
− MOD ··············· 国際規格を修正している。
2
T
3
2
11
-1
0
:
2
0
1
9
2019年7月1日の法改正により名称が変わりました。まえがきを除き、本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。

