T 0330-3:2012
(1)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
目 次
ページ
1 適用範囲 ························································································································· 1
2 引用規格 ························································································································· 1
3 用語及び定義 ··················································································································· 1
4 試薬······························································································································· 2
5 装置······························································································································· 2
5.1 溶解速度測定装置 ·········································································································· 2
5.2 ガラス電極 ··················································································································· 4
6 試料······························································································································· 4
7 溶解液の調製 ··················································································································· 4
7.1 溶解液の組成及び温度 ···································································································· 4
7.2 酢酸−酢酸ナトリウム緩衝液(pH 5.50,0.08 mol/L)の調製方法 ············································ 4
7.3 トリス(ヒドロキシメチル)アミノメタン−塩酸緩衝液(pH 7.30,0.05 mol/L)の調製方法········· 4
8 校正用カルシウム標準液の調製 ··························································································· 5
8.1 カルシウム標準液(Ca: 1 000 mg/L) ················································································· 5
8.2 pH 5.50校正用カルシウム標準液 ······················································································· 5
8.3 pH 7.30校正用カルシウム標準液 ······················································································· 5
9 試験方法 ························································································································· 6
9.1 準備操作 ······················································································································ 6
9.2 カルシウムイオン電極の校正···························································································· 6
9.3 溶解速度の試験方法 ······································································································· 6
10 試験結果の表し方 ··········································································································· 7
10.1 カルシウムイオン濃度−時間曲線 ···················································································· 7
10.2 溶解速度 ····················································································································· 7
10.3 相対溶解速度の計算 ······································································································ 7
10.4 平均値及び標準偏差 ······································································································ 7
11 報告書 ·························································································································· 8
11.1 必須項目 ····················································································································· 8
11.2 補足項目 ····················································································································· 8
T 0330-3:2012
(2)
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
まえがき
この規格は,工業標準化法に基づき,日本工業標準調査会の審議を経て,厚生労働大臣及び経済産業大
臣が制定した日本工業規格である。
この規格は,著作権法で保護対象となっている著作物である。
この規格の一部が,特許権,出願公開後の特許出願又は実用新案権に抵触する可能性があることに注意
を喚起する。厚生労働大臣, 経済産業大臣及び日本工業標準調査会は,このような特許権,出願公開後の
特許出願及び実用新案権に関わる確認について,責任はもたない。
JIS T 0330の規格群には,次に示す部編成がある。
JIS T 0330-1 第1部:多孔質バイオセラミックスの気孔構造の分析方法
JIS T 0330-2 第2部:多孔質バイオセラミックスの強度試験方法
JIS T 0330-3 第3部:溶解速度試験方法
JIS T 0330-4 第4部:りん酸カルシウム骨ペーストの物理化学的特性の測定方法
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
日本工業規格
JIS
T 0330-3:2012
生体活性バイオセラミックス−
第3部:溶解速度試験方法
Bioceramics-Part 3: Testing method of measuring dissolution rate of
calcium phosphate ceramics
1
適用範囲
この規格は,緻密体,多孔体又はか(顆)粒状りん酸カルシウム系セラミックスの溶解速度の試験方法
について規定する。
2
引用規格
次に掲げる規格は,この規格に引用されることによって,この規格の規定の一部を構成する。これらの
引用規格は,その最新版(追補を含む。)を適用する。
JIS K 0122 イオン電極測定方法通則
JIS K 0557 用水・排水の試験に用いる水
JIS K 8180 塩酸(試薬)
JIS K 8355 酢酸(試薬)
JIS K 8372 酢酸ナトリウム(試薬)
JIS K 8541 硝酸(試薬)
JIS K 8617 炭酸カルシウム(試薬)
JIS K 9704 2-アミノ-2-ヒドロキシメチル-1, 3-プロパンジオール(試薬)
JIS R 1600 ファインセラミックス関連用語
JIS R 3503 化学分析用ガラス器具
JIS Z 8401 数値の丸め方
JIS Z 8802 pH測定方法
JIS Z 8805 pH測定用ガラス電極
3
用語及び定義
この規格で用いる主な用語及び定義は,JIS R 1600によるほか,次による。
3.1
カルシウムイオン電極
カルシウムイオン電極は,溶液中のカルシウムイオン活量に応答し,電位を発生する電極。カルシウム
イオン選択性電極ともいう。
2
T 0330-3:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
3.2
比較電極(参照電極)
比較電極(参照電極)は,標準水素電極に対して電位が既知であって,電位が安定している電極。カル
シウムイオン電極の電位を測定又は制御するために対極として用いられる(JIS K 0122参照)。
3.3
複合電極
複合電極は,イオン電極又はpH電極に比較電極を組み込んだもの。
3.4
AD変換器
センサーのアナログ測定値を連続的に取り込んで,デジタル値に変換して出力するアナログ−デジタル
変換器。
4
試薬
4.1
水 JIS K 0557に規定するA2又はA3の水。
4.2
塩酸 JIS K 8180に規定する特級用。
4.3
硝酸 JIS K 8541に規定するもの。
4.4
酢酸 JIS K 8355に規定するもの。
4.5
酢酸ナトリウム JIS K 8372に規定するもの。
4.6
炭酸カルシウム JIS K 8617に規定するもの。
4.7
2-アミノ-2-ヒドロキシメチル-1, 3-プロパンジオール[トリス(ヒドロキシメチル)アミノメタン]
JIS K 9704に規定するもの。以下,トリス(ヒドロキシメチル)アミノメタンという。
5
装置
5.1
溶解速度測定装置
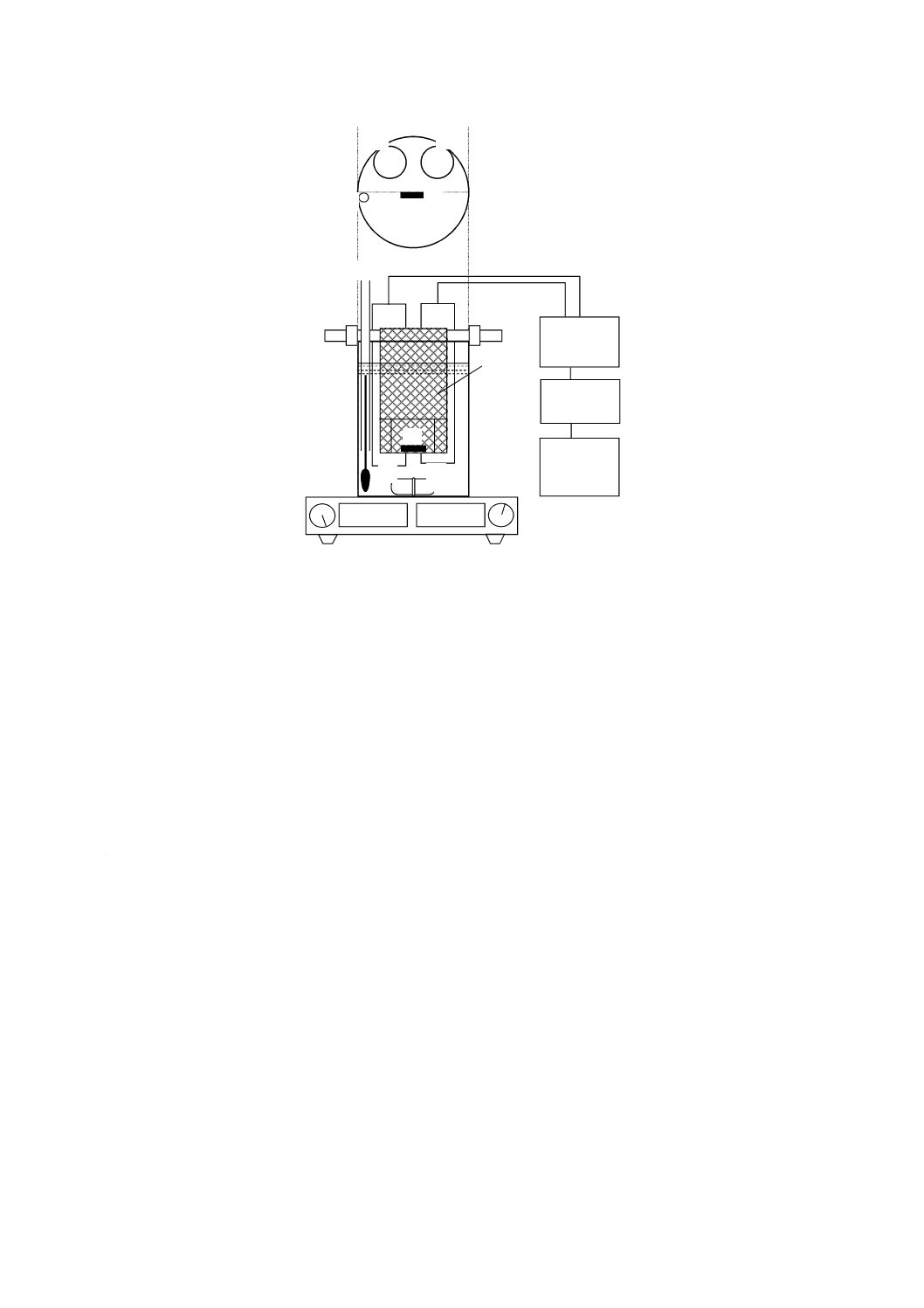
溶解速度測定装置は,カルシウムイオン電極,比較電極(参照電極),イオン濃度計,溶解液容器,マグ
ネチックスターラー,AD変換器,記録計などからなる。その基本構成の例を,次に示す(図1参照)。
3
T 0330-3:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
①
②
③
④
②
③
⑤
④
⑥
⑨
⑩
⑪
①
rpm
˚C
⑧
⑦
① 試料
② カルシウムイオン電極
③ 比較電極(参照電極)
④ 温度計
⑤ プラスチック製ネット
⑥ 回転子
⑦ 溶解液容器
⑧ マグネチックスターラー
⑨ イオン濃度計
⑩ AD変換器
⑪ 記録計
図1−溶解速度測定装置の構成例
a) カルシウムイオン電極 JIS K 0122に規定する定量範囲[0.4〜4 000 mg/L(mg/dm3)]及び測定pH範
囲(pH 5〜8)をもつもの。
b) 比較電極(参照電極) 標準水素電極に対して電位が既知であって,電位が安定している電極。a)の
カルシウムイオン電極が複合電極の場合は,比較電極は,使用しない。
注記 用いる比較電極は,二重液絡形が好ましい。
c) イオン濃度計 カルシウムイオン電極の応答電位を測定するための,高入力抵抗[1 TΩ以上(T: 1012)]
の直流電位差計。測定電位又はデータ処理によってイオン濃度に変換した値を,デジタル又はアナロ
グ出力できるもの。
d) マグネチックスターラー 回転速度(rpm)を表示できるもの。
e) AD変換器 イオン濃度計がアナログ出力の場合に用いる。
f)
記録計 イオン濃度計又はAD変換器の出力するデジタルデータを,連続的に記録する装置。測定デ
ータと時間データとを同時に記録できるインタフェース及びソフトウェアをもつもの。
4
T 0330-3:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
g) 溶解液容器 JIS R 3503に規定するビーカー100 mLとする。
5.2 ガラス電極
pH計のガラス電極は,JIS Z 8805に規定するものを用いる。
6
試料
使用する試料は,緻密体,多孔体又はか(顆)粒とする。あらかじめ,溶解速度を試験するテスト試料
と,溶解速度の比較対照にするコントロール試料とを定めておく。試料1個の質量は,100±1 mgとする。
テスト試料及びコントロール試料とも,各々5個以上を準備する。
注記 試料がか粒の場合は,合計質量100±1 mgのか粒全量を1個の試料とみなす。
7
溶解液の調製
7.1
溶解液の組成及び温度
試料を浸せきして溶解速度を試験する溶解液は,酢酸−酢酸ナトリウム緩衝液(pH 5.50,0.08 mol/L)
とする。トリス(ヒドロキシメチル)アミノメタン−塩酸緩衝液(pH 7.30,0.05 mol/L)を用いてもよい。
使用する溶解液は,100±0.1 mL,温度は25±3 ℃とする。
7.2
酢酸−酢酸ナトリウム緩衝液(pH 5.50,0.08 mol/L)の調製方法
酢酸−酢酸ナトリウム緩衝液(pH 5.50,0.08 mol/L)の調製は,次による。
a) 酢酸(0.8 mol/L) 酢酸4.804 g(0.08 mol)をはかりとり,全量フラスコ100 mLに移し入れ,水を標
線まで加えて調製する。
b) 酢酸ナトリウム溶液(0.8 mol/L) 酢酸ナトリウム65.62 g(0.8 mol)をはかりとり,全量フラスコ
1 000 mLに移し入れ,水を標線まで加えて調製する。
c) 酢酸−酢酸ナトリウム緩衝液(pH 5.50,0.8 mol/L) a)で調製した酢酸溶液(0.8 mol/L)1 mL及び
b)で調製した酢酸ナトリウム溶液(0.8 mol/L)X mLを採取して“試し混合”してpHを測定し,25±
3 ℃でpHが5.50±0.02になるXを求める。Xは,約6〜7 mLの値となる。25±3 ℃で,残りの酢酸
溶液と酢酸ナトリウム溶液とを混合比1:Xで混合し,酢酸−酢酸ナトリウム緩衝液(pH 5.50±0.02,
0.8 mol/L)とする。
d) 酢酸−酢酸ナトリウム緩衝液(pH 5.50,0.08 mol/L) c)で調製した酢酸−酢酸ナトリウム緩衝液(pH
5.50,0.8 mol/L)を水で10倍に希釈する。
7.3
トリス(ヒドロキシメチル)アミノメタン−塩酸緩衝液(pH 7.30,0.05 mol/L)の調製方法
トリス(ヒドロキシメチル)アミノメタン−塩酸緩衝液(pH 7.30,0.05 mol/L)(トリス−塩酸緩衝液と
もいう。)の調製は,次による。
a) トリス(ヒドロキシメチル)アミノメタン溶液(0.05 mol/L) トリス(ヒドロキシメチル)アミノ
メタン6.057 g(0.05 mol)をはかりとり,全量フラスコ1 000 mLに移し入れ,水を標線まで加えて調
製する。
注記 2 L以上のトリス(ヒドロキシメチル)アミノメタン溶液(0.05 mol/L)を調製する場合,こ
の操作を繰り返し,これらの溶液を一つの溶液に混合する。
b) トリス(ヒドロキシメチル)アミノメタン−塩酸緩衝液(pH 7.30,0.05 mol/L) a)で調製したトリ
ス(ヒドロキシメチル)アミノメタン溶液(0.05 mol/L)を,かくはんしながら25±3 ℃でpHを測定
しつつ,塩酸を徐々に滴下し,トリス(ヒドロキシメチル)アミノメタン溶液(0.05 mol/L)のpHを
pH 7.30±0.05に調製する。
5
T 0330-3:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
注記 用いる塩酸は,JIS K 8180に規定する塩酸8.33 mLをはかりとり,水で希釈して100 mLとし
た塩酸(1 mol/L)でもよい。
8
校正用カルシウム標準液の調製
8.1
カルシウム標準液(Ca: 1 000 mg/L)
カルシウム標準液(Ca:1 000 mg/L)は,硝酸(0.1 mol/L)に1 000 mg/Lのカルシウムイオンを含有す
るものとする。
注記 カルシウム標準液(Ca:1 000 mg/L)は,以下のようにして調製できる。炭酸カルシウムを105
±2 ℃で約2時間加熱し,デシケーター中で放冷する。その2.497 gをはかりとり,硝酸(1 mol/L)
(硝酸75 mLを水に溶かして1 Lとする。)100 mLに溶かし,沸騰しない程度に数分間加熱し
て二酸化炭素を除去する。放冷後,全量フラスコ1 000 mLに移し入れ,水を標線まで加える。
8.2
pH 5.50校正用カルシウム標準液
8.1のカルシウム標準液(Ca:1 000 mg/L)と7.2 c)の酢酸−酢酸ナトリウム緩衝液(pH 5.50,0.8 mol/L)
とを表1に規定する量だけ全量フラスコ100 mLに移し入れ,水を標線まで加えて,カルシウムの濃度
1 mg/L,10 mg/L及び100 mg/Lの酢酸−酢酸ナトリウム緩衝液(pH 5.50,0.08 mol/L)を調製する。
表1−pH 5.50校正用カルシウム標準液の調製方法(混合割合)
単位 mL
カルシウムの濃度
(mg/L)
カルシウム標準液
(Ca:1 000 mg/L)
酢酸−酢酸ナトリウム緩衝液
(pH 5.50,0.8 mol/L)
水
(100 mLにするのための理論値)
1
0.10
10.0
89.9
10
1.00
10.0
89.0
100
10.0
10.0
80.0
8.3
pH 7.30校正用カルシウム標準液
8.1のカルシウム標準液(Ca: 1 000 mg/L)1.00 mLを全量フラスコ200 mlにとり,7.3 b)のトリス(ヒド
ロキシメチル)アミノメタン−塩酸緩衝液(pH 7.30,0.05 mol/L)を標線まで加える。この溶液を全量フ
ラスコ100 mLを用いて,7.3 b)のトリス(ヒドロキシメチル)アミノメタン−塩酸緩衝液(pH 7.30,
0.05 mol/L)で表2のように2倍希釈及び10倍希釈して,カルシウムの濃度0.5 mg/L,2.5 mg/L及び5.0 mg/L
のトリス(ヒドロキシメチル)アミノメタン−塩酸緩衝液(0.05 mol/L)とする。
表2−pH 7.30校正用カルシウム標準液の調製方法(混合割合)
単位 mL
カルシウム
の濃度
(mg/L)
カルシウムの濃度5.00 mg/Lの
トリス−塩酸緩衝液
(pH 7.30,0.05 mol/L)
トリス−塩酸緩衝液(pH 7.30,0.05 mol/L)
(100 mLにするのための理論値)
0.5
10.0
90.0
2.5
50.0
50.0
5.0
残り140.0
0(希釈なし)
6
T 0330-3:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
9
試験方法
9.1
準備操作
製造業者が指示するカルシウムイオン電極の取扱い方法及びJIS K 0122の表2(イオン電極及び比較電
極の使い始め,保存,再生,取扱い上の注意の一例)に規定する使い始めの注意事項に従って,あらかじ
め準備操作(水道水に浸しておくなど)を実施する。カルシウムイオン電極,イオン濃度計及び記録計を
接続して,オンラインでデータを取り込めるようにする。
9.2
カルシウムイオン電極の校正
カルシウムイオン電極の校正は,校正用カルシウム標準液(8.2又は8.3)を用いて,25±3 ℃でJIS K 0122
の6.4.1(絶対検量線法)に規定する絶対検量法によって行う。必ずカルシウム濃度の低いものから順に校
正する。表示値が安定するまで(4〜6分間)十分に時間をかけて校正する。
注記 カルシウムイオン電極は,経時的に劣化する。正常なカルシウムイオン電極は,Log[Ca濃度
(mg/L)]と電極の応答電位(mV)とがほぼ直線関係になり,理論的には,25 ℃でカルシウ
ムイオン活量が10倍変化すると,応答電位は29.58 mV変化する。カルシウムイオン電極が劣
化した場合は,このような直線関係が得られないか又は表示値が一定値に収束しない。
9.3
溶解速度の試験方法
箇条6のテスト試料及びコントロール試料の溶解速度の測定は,次による。
a) 試料(100±1 mg)をプラスチック製ネットに入れてつり下げ,溶解液注入前の容器中心に取り付け
る。試料は,磨耗及び破壊が起こらないように配置する。とりわけ,試料は,回転子と接触しないよ
うにする。
b) 次に,カルシウムイオン電極を容器内にセットし,25±3 ℃の溶解液100±0.1 mLを容器に注入し,
イオン濃度計の製造業者が指示する回転数で回転子を回転させた後,溶解液と試料とが接触してから
1分以内に,溶解液カルシウムイオンの濃度のオンラインデータの取り込みを開始する。
c) そのまま,溶解液中のカルシウムイオンの濃度のオンラインデータを,2分間隔で30分間測定する。
測定中にカルシウムイオンの濃度が表3に規定する濃度範囲を超えた場合は,その時点で測定を終了
する。
d) 測定終了後,校正用カルシウム標準液のカルシウムイオンの濃度,及び溶解液のpHを測定する。pH
の測定は,JIS Z 8805に規定する電極を用いて,JIS Z 8802によって測定する。
e) d)で測定した校正用カルシウム標準液のカルシウムイオンの濃度と標準液本来のカルシウムイオン濃
度との差が,2点以上で本来のカルシウムイオン濃度の±10 %を超える場合は,取り込んだオンライ
ンデータを破棄し,カルシウムイオン電極を再校正し,新しい試料を用いて再測定する。
f)
d)で測定した溶解液が,pH 5.50の場合はpH 5.50±0.03,pH 7.30の場合はpH 7.30±0.06を逸脱した
ときは,取り込んだオンラインデータを破棄し,カルシウムイオン電極を再校正し,新しい試料を用
い,測定時間を短縮して再測定する。
g) いずれのpHの場合でも,テスト試料とコントロール試料とを各々5個以上用いて,各々5回以上の独
立したオンラインデータを取得する。
h) 溶液のかき混ぜ状態は,カルシウムイオン電極の応答電位,応答速度及び定量下限の変化となって影
響を与えるため,かき混ぜ速度,容器内での試料,イオン電極及び回転子の位置は,全ての試料で一
定になるようにし,できる限り試料間のかき混ぜ状態を一定にする。
7
T 0330-3:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
表3−測定時のカルシウムイオン濃度範囲
単位 mg/L
試料の材質
pH 5.50
pH 7.30
水酸アパタイトセラミック
0.4〜6
−
(0〜0.2 )a)
β-りん酸三カルシウムセラミック
0.4〜10
0.4〜1
水酸アパタイト−β-りん酸三カル
シウム2相セラミック
0.4〜
b)
×
+
×
100
10
100
6
TCP
HA
0〜
c)
b)
×
+
×
100
0.1
100
2.0
TCP
HA
注a) カルシウムイオンの検出下限濃度が0.2 mg/L以下のカルシウムイオン電極を用いた場合に測定可能。
b) HA:水酸アパタイトの含有量(質量百分率) TCP: β-りん酸三カルシウムの含有量(質量百分率)
c) 水酸アパタイトの含有量が75 %以上の場合は,カルシウムイオンの検出下限濃度が0.4 mg/L未満のカルシウム
イオン電極を用いた場合に測定可能。
10 試験結果の表し方
10.1 カルシウムイオン濃度−時間曲線
試験開始から終了までの,カルシウムイオンの濃度と溶解時間との関係を表すカルシウムイオン濃度−
時間曲線を作成する。
10.2 溶解速度
測定終了時の溶出したカルシウムイオンの量(mol),又はそれから換算した溶出試料量(mol又はg)
を測定時間(秒)で除して溶解速度を求める。
10.3 相対溶解速度の計算
テスト試料の溶解速度をコントロール試料の溶解速度で除した相対溶解速度を求める。
注記 この相対溶解速度が,骨組織内での相対吸収量をある程度反映することは,β-りん酸三カルシ
ウムセラミックについて動物実験で確認した。
10.4 平均値及び標準偏差
テスト試料又はコントロール試料の溶解速度の平均値及び標準偏差は,各々の試料の溶解速度測定値か
ら式(1)及び式(2)によって求める。
∑
=
=
n
i
i
n
x
x
1
················································································ (1)
∑
=
−
−
=
n
i
i
n
x
x
S
1
2
1
)
(
······································································ (2)
ここに,
¯x: テスト試料又はコントロール試料の溶解速度の平均値
(mol/s又はg/s)
xi: 各々の試料の溶解速度 (mol/s又はg/s)
S: 溶解速度の標準偏差 (mol/s又はg/s)
n: 試料の個数
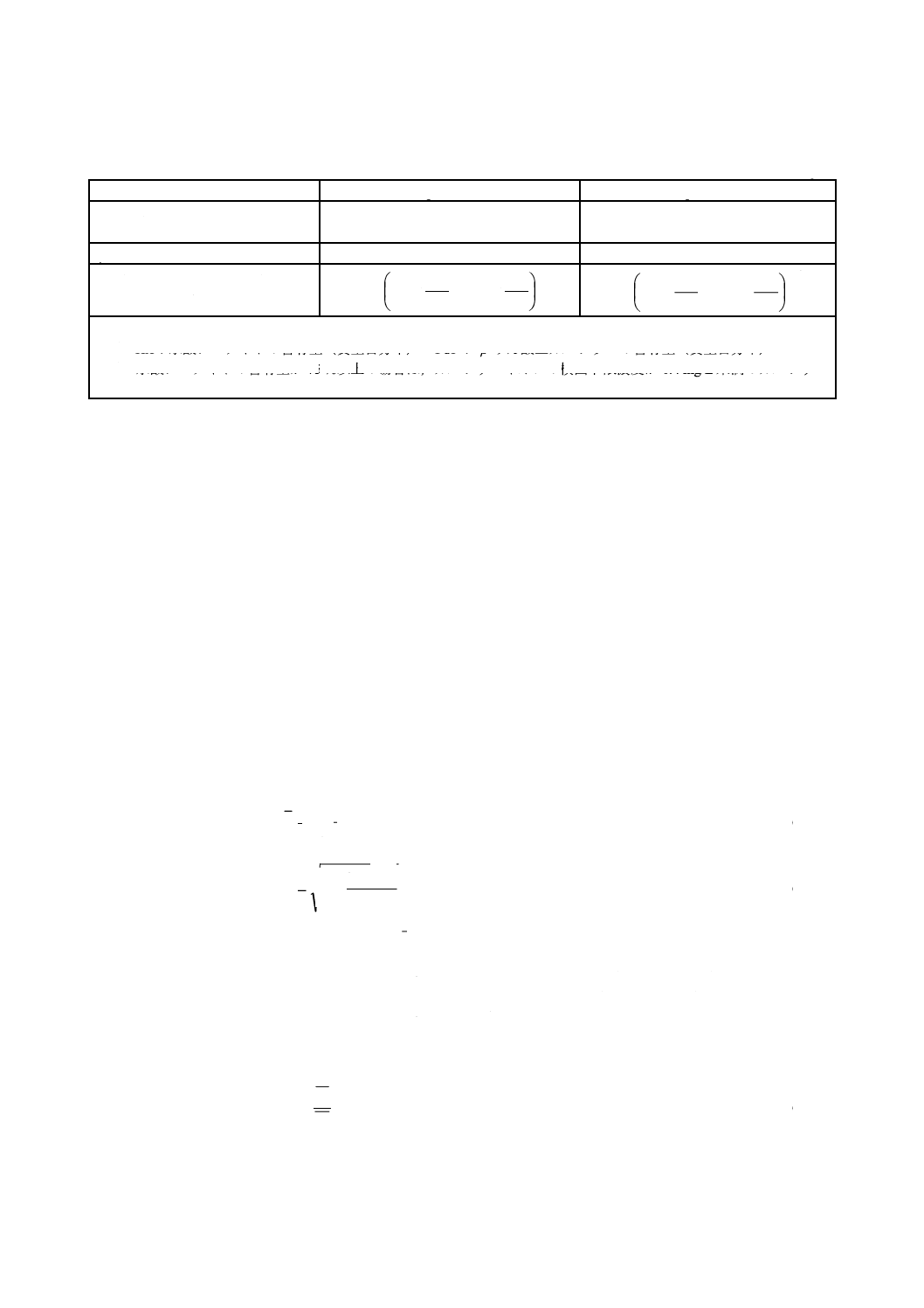
相対溶解速度の平均値及び標準偏差は,テスト試料及びコントロール試料の溶解速度平均値及び標準偏
差を用いて式(3)及び式(4)によって求める。
0
t
r
x
x
x=
···················································································· (3)
8
T 0330-3:2012
2019年7月1日の法改正により名称が変わりました。まえがきを除き,本規格中の「日本工業規格」を「日本産業規格」に読み替えてください。
()
+
−
=
2
t
0
2
0
2
2
0
t
r
1S
x
S
x
x
S
···················································· (4)
ここに,
¯¯xr: 相対溶解速度の平均値 (mol/s又はg/s)
¯¯xt: テスト試料の溶解速度の平均値 (mol/s又はg/s)
¯¯x0: コントロール試料の溶解速度の平均値 (mol/s又はg/s)
St: テスト試料の溶解速度の標準偏差 (mol/s又はg/s)
S0: コントロール試料の溶解速度の標準偏差(mol/s又はg/s)
Sr: 相対溶解速度(¯¯xt/¯¯x0)の標準偏差
計算した溶解速度及び相対溶解速度の平均値及び標準偏差は,JIS Z 8401によって,有効数字2桁に丸
める。
11 報告書
11.1 必須項目
試験報告書には,次の事項について記載する。
a) この規格番号
b) 試験年月日,試験場所及び試験者名
c) 材料の名称,種類及び化学組成
d) 試料形状,寸法及び質量
e) 試料の気孔率及び平均気孔径
f)
試料の個数
g) 溶解液の種類,pH及び温度
h) 溶解試験条件(溶解時間,かくはん速度,回転子の大きさ,電極,回転子及び試料の位置関係)
i)
カルシウムイオン電極,比較電極及びイオン濃度計の名称及び形式
j)
溶解液の最終pH(9.3参照)
k) 溶解速度測定終了後に測定した,校正用カルシウム標準液のカルシウムイオン濃度(9.3参照)
l)
試験結果(カルシウムイオン濃度−時間曲線)
m) 溶解速度の平均値及び標準偏差
n) m)の溶解速度が溶出カルシウムの量によるものか,又は溶出試料量によるものかの区別
o) 相対溶解速度の平均値及び標準偏差
11.2 補足項目
次の各項目を付け加えて報告することが望ましい。
a) 材料の製造業者名及び製造年月日
b) 材料の添加物の種類及び焼結方法
c) 素材からの試料の採取条件及び加工条件
d) 温度,湿度などの試験環境条件


